Nat Chem Biol:精准“拆弹”!科学家用化学小分子揪出癌细胞的“总开关”,让肺癌肿瘤生长急刹车!
这项研究首次通过化学方法精确“解码”了特定HAT复合物的功能,揭示了ATAC在维持癌症基因表达程序中的独特作用。
人体每个细胞都包含一套完整的生命密码—DNA,但决定这些密码何时启动的,往往不是密码本身,而是一套复杂的“开关系统”。这套系统就是表观遗传调控,其能通过给DNA的“线轴”—组蛋白添加或移除化学标记,来决定基因是“开启”还是“沉默”。其中组蛋白乙酰化是最重要的“启动开关”之一,负责催化这个反应的“开关操作员”,就是组蛋白乙酰转移酶复合物。
近日,一篇发表在国际杂志Nature Chemical Biology上题为“Complex-specific inhibitors for interrogating ATAC histone acetyltransferase complex”的研究报告中,来自香港大学等机构的科学家们通过研究设计出了一种名为LS-170的化学抑制剂,其就像一枚精准的“导弹”,能击中肺癌细胞中一个名为ATAC复合物的关键调控器,令其失去激活促癌基因的能力。

ATAC复合物就是其中一位关键“操作员”,它专门负责激活与细胞生长、DNA复制相关的基因。在正常的细胞中,这套开关系统井然有序。但在非小细胞肺癌这类癌症中,ATAC复合物却变得异常活跃。它像是被卡在“开启”位置,不断激活大量促癌基因,驱动肿瘤疯狂生长和转移。肺癌是全球癌症死亡的首要原因,据世界卫生组织数据,每年约有180万人死于肺癌,其中非小细胞肺癌占所有肺癌病例的85%。面对这样的对手,传统的“一刀切”式药物往往效果有限,且副作用明显。
从“拆弹”到“精准拆除”
过去,药物研发的思路是直接瞄准ATAC复合物中的“剪刀手”GCN5,它负责为组蛋白添上乙酰化标记;但问题是,GCN5并非ATAC独有,它还服务于细胞内其他几个重要的复合物。直接抑制GCN5就像为了关掉一个坏掉的开关,而把整个电闸都拉断了,这必然会干扰细胞正常功能,带来巨大副作用。
这项研究中,研究人员通过联合研究,共同构思了一个更为精巧的策略:不攻击共享的“工具”,而是靶向ATAC复合物特有的“把手”。这个“把手”就是YEATS2蛋白亚基。利用结构导向的合理药物设计,研究团队成功开发出一种高效、高选择性的YEATS2抑制剂,并将其命名为LS-170。
LS-170能精准地结合到YEATS2的特定结构域上,阻止其将整个ATAC复合物“锚定”在染色质上;这样一来,ATAC复合物便从它本该控制的基因组区域上被“驱逐”了。这就像精准拆除了坏开关的固定底座,让它无法工作,而其他好开关的底座完好无损,不受影响。
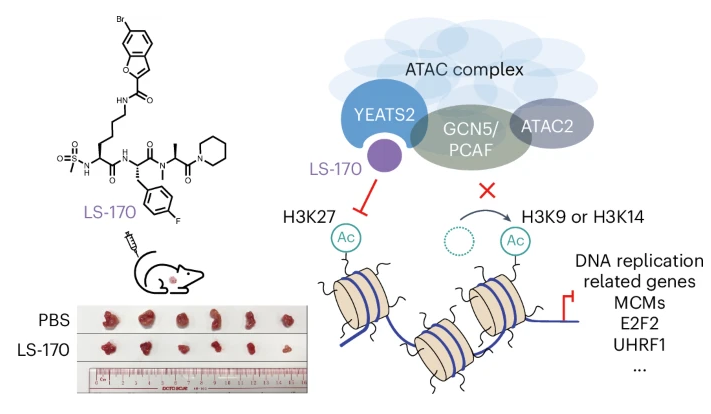
在非小细胞肺癌细胞系和动物模型中,LS-170展现出了强大的抗肿瘤功效。实验结果显示,LS-170能显著降低ATAC复合物在染色质上的占据率,减少其依赖的组蛋白乙酰化水平,并下调由ATAC掌控的基因表达,最终结果令人振奋:肿瘤的生长和转移被显著抑制。
研究者表示,在这项工作中,他们不仅创造了一种能够抑制肿瘤的强效、高选择性抑制剂,还揭示了一种全新策略:在多个共享同一酶核心的复合物中,仅精准靶向其中一个。值得一提的是,YEATS2基因在包括肺癌、卵巢癌和胰腺癌在内的多种实体瘤中频繁扩增。这意味着,这种靶向策略可能具有超越肺癌治疗的更广泛潜力。
这项研究首次通过化学方法精确“解码”了特定HAT复合物的功能,揭示了ATAC在维持癌症基因表达程序中的独特作用。它不仅为肺癌治疗提供了全新的潜在策略,也为开发针对其他疾病的、复合物特异性的表观遗传药物提供了全新思路。这项工作开启了一种令人兴奋的可能性:开发高选择性、复合物特异性的药物,或将彻底改变人类疾病的治疗方式。
从科学突破到临床应用,道路依然漫长,LS-170需要在更多临床前模型中进行验证,并最终通过严格的临床试验才能评估其对人体的安全性和有效性;但毋庸置疑,这项研究为对抗肺癌等癌症,点亮了一盏充满希望的引路之灯。
参考文献:
Liu, S., Liu, J., Wu, Y. et al. Complex-specific inhibitors for interrogating ATAC histone acetyltransferase complex. Nat Chem Biol (2026). doi:10.1038/s41589-025-02132-7
来源:生物谷