央广网北京5月6日消息(记者彭扬)5月6日,国家药品监督管理局发布2026年5月6日药品批准证明文件送达信息,本批次共有100个受理号,涉及多款新药或新适应证。
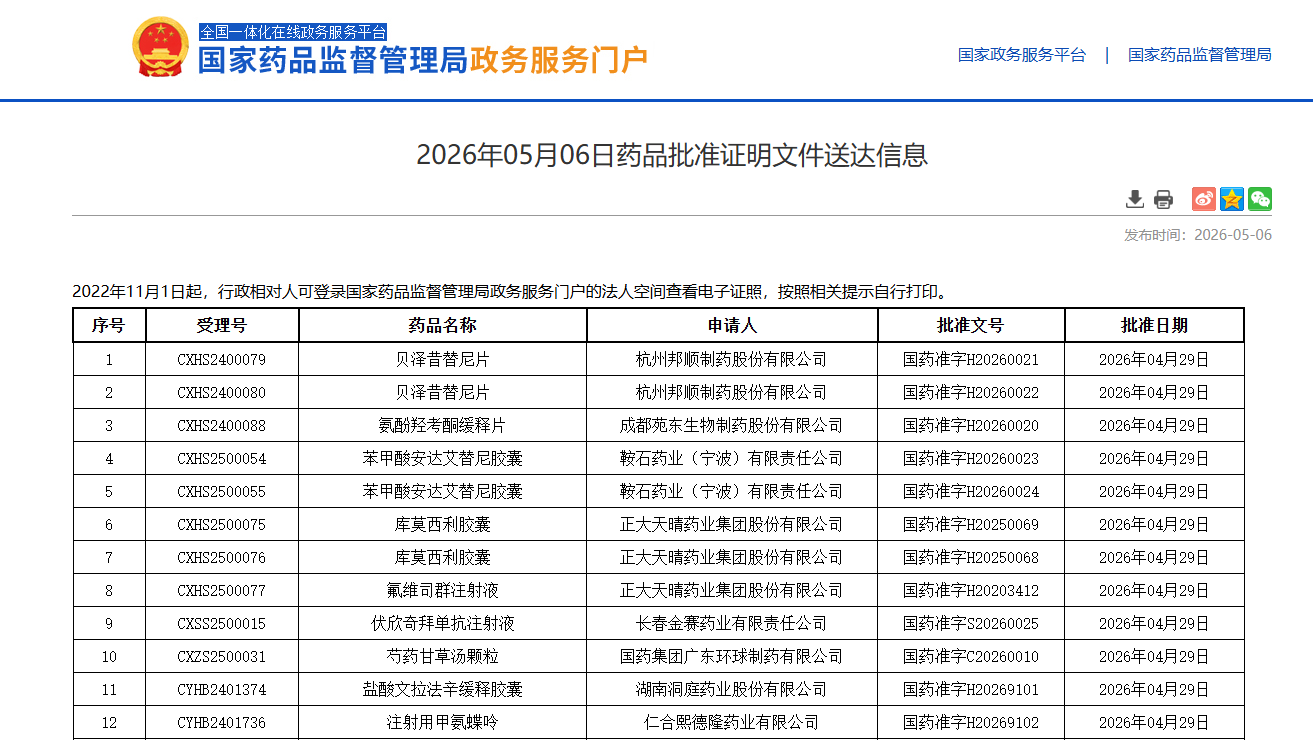
部分药品批准证明文件送达信息。来源:国家药监局官网截图
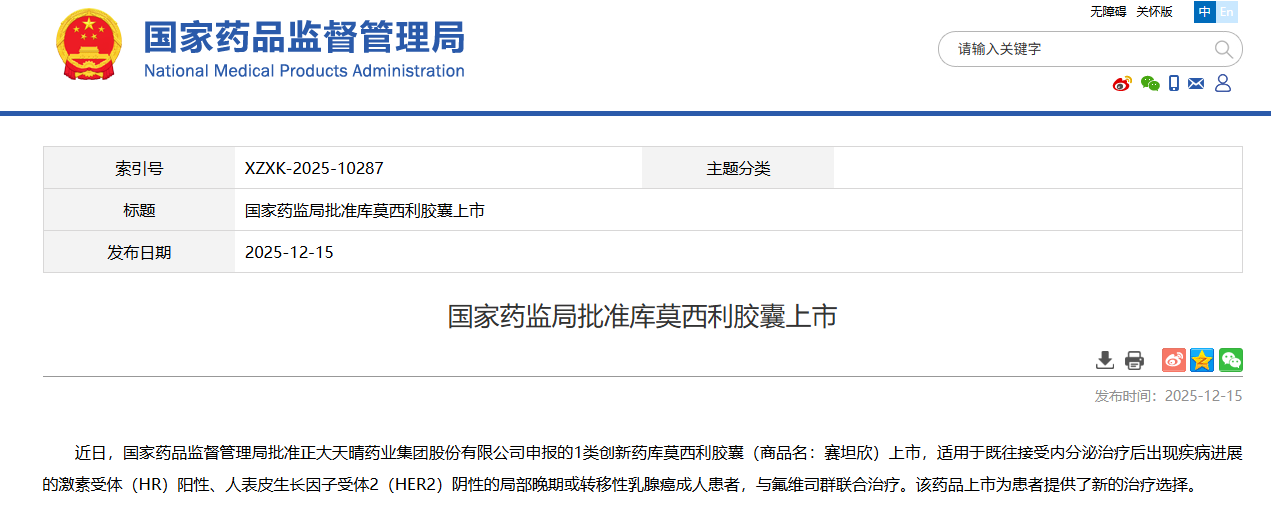
其中,正大天晴药业自主研发的库莫西利胶囊新适应证获得批准,联合氟维司群用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌患者的初始治疗。据了解,这是库莫西利胶囊获批上市的第2个适应证。去年12月,库莫西利已获批联合氟维司群用于既往接受内分泌治疗后出现疾病进展的HR+/HER2-乳腺癌适应证。
此次发布的还有国家药监局已公告的多款新药批件。其中,杭州邦顺制药的1类创新药贝泽昔替尼片获批上市,用于中危-2或高危的原发性骨髓纤维化(PMF)、真性红细胞增多症继发的骨髓纤维化(PPV-MF)或原发性血小板增多症继发的骨髓纤维化(PET-MF)成年患者的一线治疗,治疗疾病相关脾肿大或改善疾病相关症状。
鞍石药业(宁波)的1类创新药苯甲酸安达艾替尼胶囊附条件批准上市,该药适用于既往经含铂化疗治疗时或治疗后出现疾病进展,或不耐受含铂化疗,并且经检测确认存在表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者。